聚焦干细胞新药开发及临床转化,赛隽生物首个干细胞注射液产品获批临床

2021年12月8日,广州赛隽生物科技有限公司(以下简称“赛隽生物”)自主研发的CG-BM1异体人骨髓间充质干细胞注射液(受理号CXSL2101334),正式获得国家药品监督管理局药品审评中心的药物临床试验批准。CG-BM1获批的临床研究适应症为:感染引起的中重度成人急性呼吸窘迫综合征(ARDS)。
此次IND获批,标志着赛隽生物干细胞新药将从研发走向临床,是赛隽生物新药研发管线的重要里程碑。
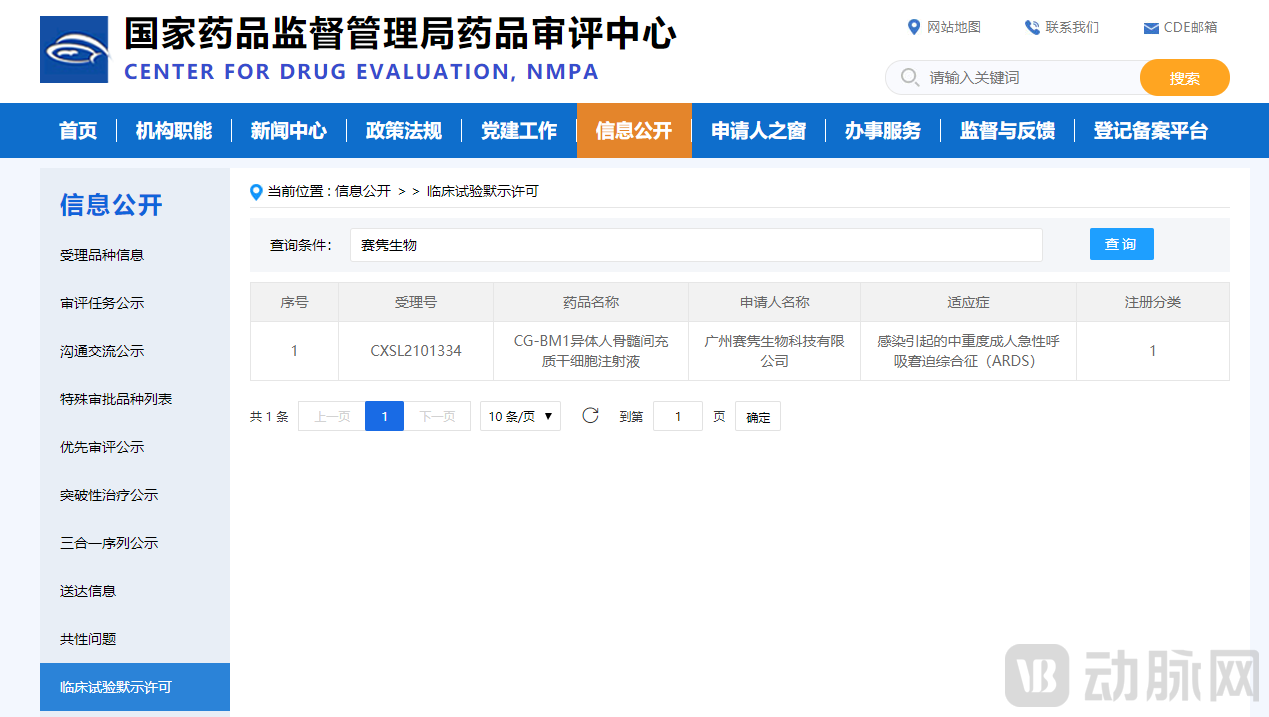
赛隽生物“CG-BM1异体人骨髓间充质干细胞注射液”获临床试验默示许可
“在干细胞药物市场,目前全国拿到IND批件的项目有20多个,我们是广东省的第二家。”赛隽生物联合创始人沈于阗博士表示,“这是我们的第一个IND获批,对于我们来说意义重大。首先是验证了我们的干细胞平台体系真正地搭建起来并且行之有效。其次,通过完整的申请过程,熟悉了申报流程,积累了团队经验,有了第一个的成功,未来才能有第10个,第100个的成功。”
赛隽生物成立于2016年3月,是一家聚焦干细胞新药开发及临床转化的干细胞技术公司。该公司目前已组建一支由20多位科学家组成的产学研医新型研发团队,并与相关科研院所建立紧密的合作关系,拥有专业的项目管理人员和产业化技术人员。
公司构建了干细胞研发、中试、生产、质量的完整技术体系,拥有设施齐备的研究生产基地,建有符合GMP标准的干细胞临床转化平台实验室3000㎡,干细胞制剂生产能力达到3000份/年。
国内有丰富的干细胞技术成果,但缺乏转化的桥梁
随着中国老龄化程度不断加深,以及人们饮食、作息等生活方式的改变,许多重大难治型疾病发病率呈现爆炸式上升趋势,比如肿瘤,神经系统疾病等,在目前还没有非常好的治疗手段。
干细胞是一类具有自我更新和多向分化潜能的细胞,拥有超强的再生、修复能力。基于其独特的生物特性,干细胞技术在植入后的局部微环境分泌不同功能的细胞因子,尤其在调控免疫和炎症反应,促进细胞和组织修复方面展现出独特的临床应用前景。
沈博士表示:“干细胞的特性带来了非常大的想象空间,以干细胞为代表的的新型治疗方式,在多种难治性疾病上展现了良好的应用前景,因此干细胞产品开发已成为新的竞争热点,市场空间巨大。”
数据显示,预计2024年全球干细胞医疗潜在市场规模将达到3614亿美元。
在世界范围内,干细胞领域已有多次跨国并购开展。2015年4月,富士胶片控股株式会社以3.07亿美金全资收购干细胞公司Cellular Dynamics International。2019年9月,Vertex Pharmaceuticals以9.5亿美元收购生物技术公司Semma Therapeutics,开发干细胞衍生的人类胰岛作为糖尿病的潜在治愈性疗法。2020年11月,诺华制药以13.5亿美元收购Mesoblast公司MSC治疗ARDS(急性呼吸窘迫症)。
间充质干细胞(MSCs)是一种成体干细胞,它具有干细胞的自我更新和多向分化特性,也是在临床应用最为广泛的一类干细胞。
自20世纪70年代被Friedenstein等人发现以来,MSCs就一直是学术界和临床转化研究的焦点。2018年有大约超过7000篇MSCs相关论文,788项已经完成或正在进行的MSCs临床研究(Ayala-Cuellar et al ., 2019)。
大量临床试验已证实MSC对多种与衰老相关的疾病均具有非常良好的治疗效果,包括肝损伤、脑功能减退、软骨损伤、男性迟发性性腺功能减退症、卵巢早衰等。
目前,在间充质干细胞领域,从科研项目申请专利数量,开展干细胞相关临床研究数量以及发表的论文来看,中国的干细胞学术成果处于世界第二,仅次于美国。
国内有很好的干细胞技术成果,却缺乏转化的桥梁。
据沈博士介绍:“真正从干细胞技术形成的药物来看,国际上批准上市的干细胞产品共13个,其中9款为MSC。而国内还没有干细胞产品上市。通过调研分析我们发现,国内干细胞研究领域缺乏成熟的科研成果转化桥梁,这也孕育了一个非常重要的商业机会。”
聚焦干细胞新药开发及成果转化平台搭建
赛隽生物的核心团队成员来自于公司首席科学家项鹏教授所在的中山大学干细胞研发团队。
项鹏教授20多年深耕于干细胞的基础与转化研究,是中山大学教授、博士生导师,也是间充质干细胞标准的牵头制定者。
在2016年以前,国内有许多关于干细胞的研究,但是总体规模较小,也缺乏行业性的指导标准。当时国内干细胞研究者面临的困难是有拥有干细胞技术成果,应用前景广阔,却找不到一家公司能够完成实验室成果的转化。
从制定工业化标准,到中试产品开发,药物研究,药物安全性评价报告,最后申请IND,需要强大且完整的工艺开发转化和重复实验能力。
为了解决这个痛点问题,2016年3月,赛隽生物成立,通过6年的潜心努力,聚焦于干细胞新药开发及临床转化,建立了一套完整的技术和工艺体系,覆盖干细胞完整产业链条的工艺开发、生产制备及质量控制体系。
此外,赛隽生物正着手开展干细胞规模化扩增工艺的开发,努力构建成本优势,同时也从产品质量上提高了干细胞成药的可能性。
开发三代MSC产品,挑战重大难治性疾病
赛隽生物将第一代MSC产品定义为急救药物来进行开发。第一个适应症选择定在ARDS上,不仅基于MSC的体内分布特性和药理特性,更是基于ARDS未被满足的临床需求。
2016 年 LUNG SAFE 研究显示,根据原发病严重程度,急性呼吸窘迫症(ARDS)总体院内死亡率约为40%。在我国,ICU 患者 ARDS发病率为8.2%,每年新增ARDS病例约72万。这是一类致死率高,尚无有效治疗药物的重大难治性疾病。每位患者干细胞治疗费用14万元,市场容量超过1000亿元。
在积极推进第一代MSC产品进入临床的同时,赛隽生物研究团队在强大的基础研究加持下,深入分析干细胞临床治疗局限性,并着手进行基因修饰MSC产品和定向分化MSC产品的开发,以建立产品迭代的技术优势。
提到企业的未来规划,沈博士表示希望产品在未来可以针对境内外药企开展Lisence out。
首先夯实技术是核心,加强校企合作,充分利用大学、科研院所的基础研究的结果,引进、开发、再创新,进一步丰富干细胞以及干细胞相关技术的药物管线,以及发现新的药物品种等。
二是将快速推动第一个产品于今年正式进入临床一期,尽快进入临床二期。未来希望加快多个管线的产品研发进程,三年左右进入到IPO阶段。
三是通过转化平台提供科研转化服务,一方面能通过服务获得收益,另一方面能筛选到更多更好的干细胞产品,以及有针对性的适应症,形成良性循环。
“我们花费六年时间,投入大量科研经费,建立起了这样的平台体系,不希望仅仅是只为自己服务。平台可以搭建桥梁,也有比较大的市场。希望未来能够利用我们的干细胞应用转化平台,为广大的科研工作者,提供干细胞相关科研成果和技术的转化服务,将技术变成真正的药品,真正实现让论文写在祖国的大地上,让科技成果转化以造福更多的病患。” 沈博士说。
本文来自其他网站,不代表健我头条立场和观点,如若转载,请注明出处:https://news.jianwo.com/detail_38430.html如有版权问题,请联系客服配合您删除这篇文章。
-
0

-

参与讨论

















