Healionics开发球型孔隙生物材料,实现抗阻塞抗感染的永久无针透析通路

动静脉内瘘术是一种血管融合外科手术:将前臂靠近手腕部位的动脉和邻近的静脉分别缝合至移植血管的两端,使吻合后的静脉中流动着动脉血,形成一个动静脉内瘘。动静脉内瘘能为血液透析治疗提供充足的血液,为透析治疗的充分性提供保证。
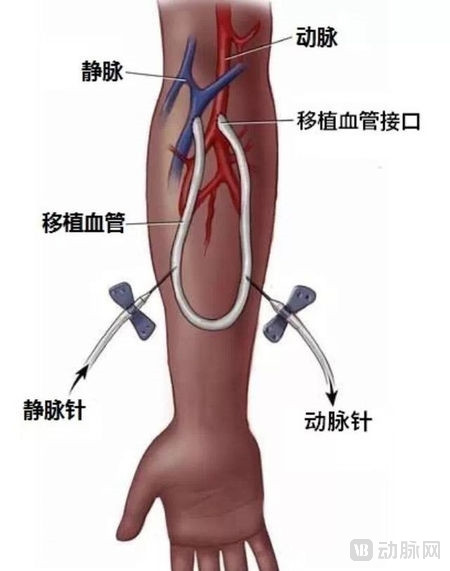
动静脉内瘘术示意图
维持性血液透析患者常用动静脉内瘘获得血管通路,但对该类病人最大的安全威胁来自与移植血管有关的血流感染(CRBSI)。在美国,超过43万依靠血液透析生存的终末期肾病患者中,每年有超5万个新的CRBSI病例发生(美国肾脏病学会临床杂志CJASN),这使有近40%的血液透析患者无法通过天然血管间的瘘管实现或维持首选的功能通路。
位于华盛顿州西雅图的医疗设备公司Healionics Corporation(以下简称Healionics)发明了一款用于动静脉内瘘术的血管移植材料,其独特的结构已被证实能够促进人体血管与其融合,并且减少感染与增生。
这款新型生物材料名为STAR®,是由美国国家工程院院士,华盛顿大学生物工程学教授与化学工程学教授、布鲁克林理工学院高分子化学博士:Buddy Ratner先生,和华盛顿大学化学工程学博士:Andrew Marshall先生共同研发。
Ratner教授在生物材料、组织工程、聚合物、生物相容性、有机材料表面分析、纳米生物技术和RF等离子体薄膜沉积方面撰写了400多篇学术著作。担任美国生物材料学会主席、AIMBE主席、国际组织工程学会(TESI)副主席,是美国科学促进会(AAAS)的会员;荣获克莱姆森生物材料文学贡献奖、材料科学Stine奖(AIChE)、韦尔奇奖(AVS)、生物材料学会霍尔奖。

STAR®生物材料发明者:Buddy Ratner教授
Marshall博士拥有斯坦福大学生物力学工程学士学位,和华盛顿大学化学工程博士学位,现任公司董事兼CTO。他在STAR®材料的技术开发及其在提高植入式医疗设备性能的应用方面拥有超过15年的经验,并为其研究成功从美国国立卫生演就演(NIH)和美国国防部获得超700万美元的竞争性非稀释性SBIR赠款。他拥有25项已颁发和正在申请的专利,并在“2012年世界组织工程与再生医学大会”上获得创新/商业化奖。

STAR®生物材料发明者,Healionics 董事兼CTO: Andrew Marshall博士
Healionics的董事长兼CEO是在医疗器械行业拥有超过30年经验的Mike Connolly先生。Connolly先生是著名企业家,风险投资家和CEO,在他创立的设备公司中有3家公司价值超20亿美元。他拥有斯坦福大学的MBA学位,麻省理工学院机械工程硕士学位和美国海军学院的学士学位。

Healionics董事长兼CEO:Mike Connolly先生
除了高水平的研发和管理团队,Healionics还吸纳了美国肾脏病学会会长Jonathan Himmelfarb博士,美国血管通路学会(VASA)创始人John Ross博士,太平洋西北血管外科学会前主席Ben Starnes博士,美国医学与生物工程学会(AIMBE)研究院成员James Bryers博士,华盛顿大学外科教授等人作为公司的医疗及科学顾问。
STAR®是一种球型孔隙生物材料。它既不是涂层也不是纳米技术,而是一种厚度为150μm及以上的3D支架。通过Healionics专有的球型工艺,不需要任何生长因子或其他生物制剂,就能在均匀分布的孔隙结构中精准实现其愈合性能。
并且,STAR®不是由牛、猪或人体组织或器官等生物材料制成。从不可降解到完全可生物降解,其可以用各种医用级合成生物基材进行生产,如硅胶、透明质酸等,以满足特定设备或应用的需求。

STAR®的球体模型结构
STAR®生物材料具有多功能性,其生物整合特性来自其专有的球型孔隙形状,而不是基材本身。因此,不同的合成技术能够将STAR®结构能被合成为血管、光盘、床单、注射颗粒等完全不同的产品类型。位于Healionics总部的实验室和洁净室生产设施能够根据客户的需求,提供有效地设计和制造定制样品的服务。

利用STAR®生物材料生产出的各式产品
STAR®其模拟细胞形状的球体结构使其在改善生物整合,减少异物反应(FBR),促进血管生成,减少疤痕组织生成方面体现出明显优势。Healionics基于此结构开发出两条产品线:血管移植物: STARgraftTM;无针透析血管通路:STARportTM。
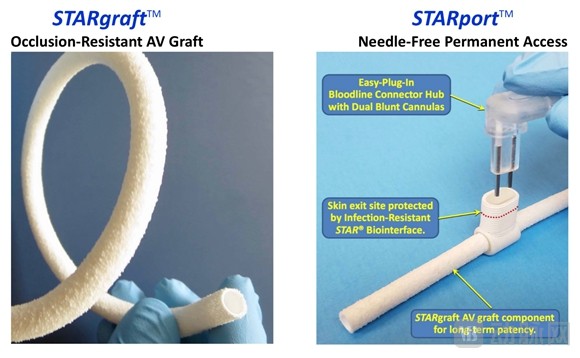
STARgraftTM:抑制增生狭窄,维持血管壁振动
抗阻塞的A型血管移植物STARgraftTM直径为6mm,共有三层结构。最内层是具有良好生物相容性的膨体材料ePTFE;最外层是命名为STARsprinklesTM的STAR®结构,其厚度为300-500μm,球型孔隙大小约为30μm;两种结构中间是硅胶粘合层。
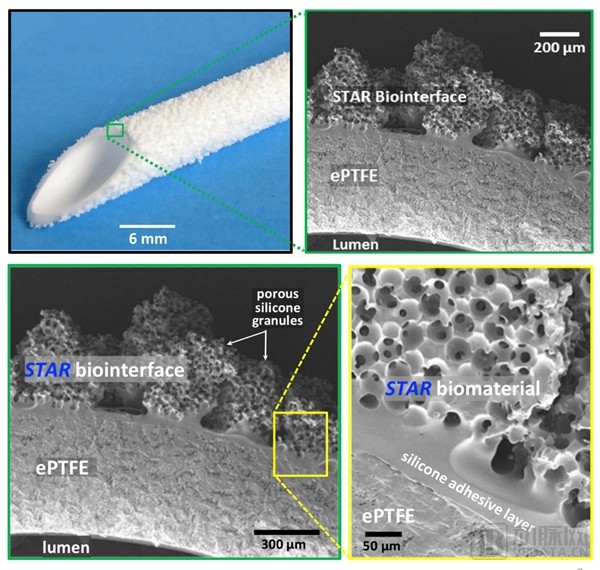
STARgraftTM具体结构展示
Andrew Marshall博士带领其团队对其表面结构的生物组织融合能力进行了动物性试验。实验结果表面:六周后,和其他两款普通硅胶移植血管相比,STARsprinklesTM的产生的异物组织更薄(<100μm)更松散,几乎不生成肉芽瘤结构。
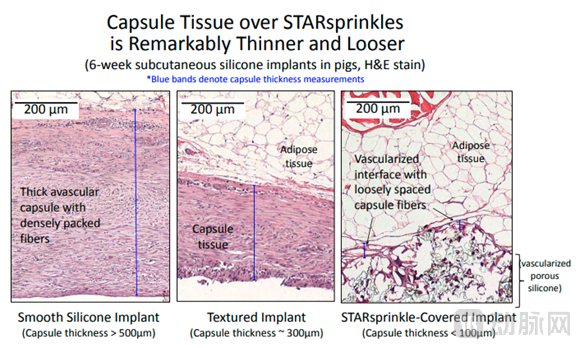
STARsprinklesTM表面几乎没有生成无血管囊结构的纤维组织
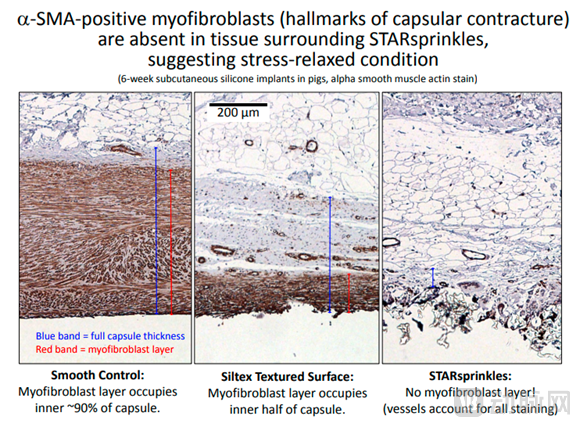
α-SMA阳性肌成纤维细胞(包膜挛缩的标志)在 STARsprinklesTM周围的组织中不存在,表明组织处于松弛状态
基于此研究成果,Marshall博士继续带领团队对STARgraftTM在血管功能实现方面做了评估。用STARgraftTM对65-80kg的羊进行动静脉内瘘手术,在实验各阶段用无创多普勒超声记录,用透视血管造影和血管内超声(IVUS)对移植物STARgraftTM进行评估。
结果表明,STARgraftTM组因增生引起的血管狭窄平均程度<10%,而对照组因增生产生的阻塞平均达到约50%,部分甚至出现完全阻塞的情况。由此证明,移植血管表面STARsprinklesTM特殊的球型孔隙可以显著减少新内膜增生引起的狭窄。此外,移植物表面附近没有生成致密的纤维囊,使植入血管维持了血管壁的振动。血管壁运动自由度的增加有助于移植血管抑制增生,改善性能。
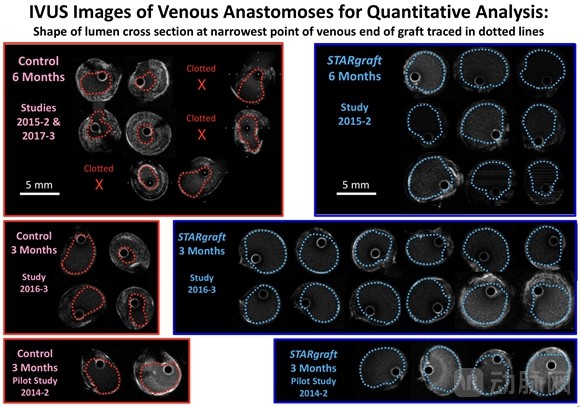
静脉吻合口的IVUS图像(虚线描绘移植体静脉端最窄处的管腔截面形状)
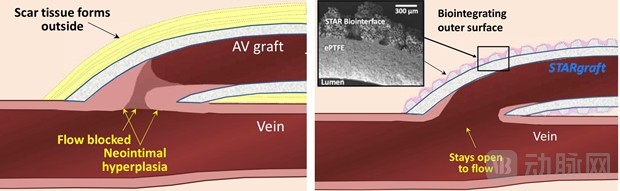
STARgraftTM解决移植血管闭塞问题示意图
STARportTM:“插座式”永久无针透析通路,助力家庭透析
在STARgraftTM的抗增生、抗阻塞以及维持血管振动方面的性能被证实后,Healionics对它进行了进一步升级,研发出无针式永久透析血管通路:STARportTM。
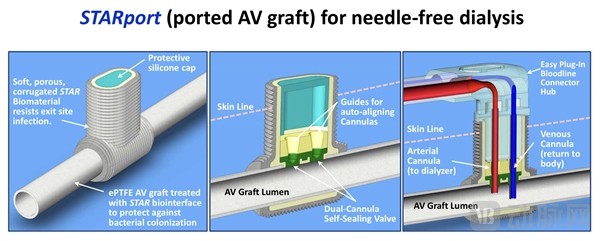
STARportTM的结构示意图
STARportTM是在STARgraftTM移植血管的基础上增设了由STARsprinklesTM材料包裹的双卡位自封式阀门接口。接口部位约10%露出于皮肤表面,与皮肤的衔接部位在STARsprinklesTM材料的作用下表现出极好的抗增生抗感染性(动物试验证实:6周内接口部位无感染且与STARportTM完全愈合)。
透析操作就像是“将插头插到插座上”:“插头部位”内置静脉插管与动脉插管,分别拥有两个非针头式钝性管口,与“插座”自封式阀门连接后,便可开始透析治疗。在两个疗程之间,将提供抗菌的软硅胶盖对接口部位进行保护。

对于Healionics来说,自团队成立到2014年,是其理论研究的主要发展阶段。科研团队在细胞形态、血管再生、皮肤病学、生物材料、皮下移植等领域发表论文或期刊50余篇。
2014年至今是各项产品的试验阶段。在猪和羊进行一系列动物实验后,2019年,STARgraftTM移植血管迎来首次人体试验。此次临床前研究表面,STARgraftTM移植血管可以改善因动静脉接口狭窄而造成的血管通路失效问题。
此后,Healionics也在继续开展进一步的人体研究,并于2021年9月2日获得来自Keiretsu Capital的470万美元融资。公司计划将该项融资用于完成STAR®系列产品的FDA市场许可, 让商业化后的产品为患者提供更安全更便捷的血液透析治疗。
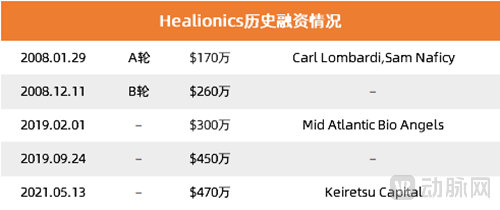
Healionics历史融资情况汇总(数据来源:crunchbase)
本文来自其他网站,不代表健我头条立场和观点,如若转载,请注明出处:https://news.jianwo.com/detail_39888.html如有版权问题,请联系客服配合您删除这篇文章。
-
0

-

参与讨论

动脉网
最近文章
相关文章
- 2022-06-26
3年净利狂增近50倍、明星机构疯抢的原料独角兽,即将登陆科创板
2022-06-25- 2022-06-21
【首发】圆因生物完成A轮融资,将加速环状RNA技术产品管线开发及临床转化
2022-06-21【首发】玄宇医疗完成亿元A轮融资,房颤PFA消融已完成首例入组
2022-06-21
关注我们
















